可以的,权限设置灵活到人,可以按照不同组织架构设置每个人或每个项目团队的权限,包括模版设置修改,实验复核,实验分享,导出文件等权限。可以让管理层随时看到所有人的实验,项目leader随时掌握自己团队的实验进展,或者研发企业时时了解CRO服务商的实验状况,老师时时关注和搜索到学生的实验记录。
法规认可电子记录等同于纸质记录,认可电子签名和电子数据。具体法规有:
1/国家食品药品监督管理总局第34号令(NMPA)2017年8月2日颁布了《药物非临床研究质量管理规范》;
2/美国FDA于1997年8月20日开始实施21 CFR Part 11:Electronic Records ; Electronic Signatures(简称Part 11);
3/欧盟地区则发布了Eudralex Volume 4, Annex 11:Computerized systems (简称Annex 11)。
了解详情,点击链接
《eCTD快来了,谈谈电子实验记录本的合规性》 ELN侧重在研究创新型实验,实验记录类型多样多变,实验内容和数据格式大多互不相同,灵活性高,专业性强。ELN可促进历史实验记录的积累,形成知识库,加速研发,多团队协作,同时符合法规要求,为企业IP和项目申报保驾护航。LIMS更多侧重在生产质量样品分析检测实验,记录固化、标准化和流程化的实验,主要是满足监管层合规性需求,而非用于促进研发创新。
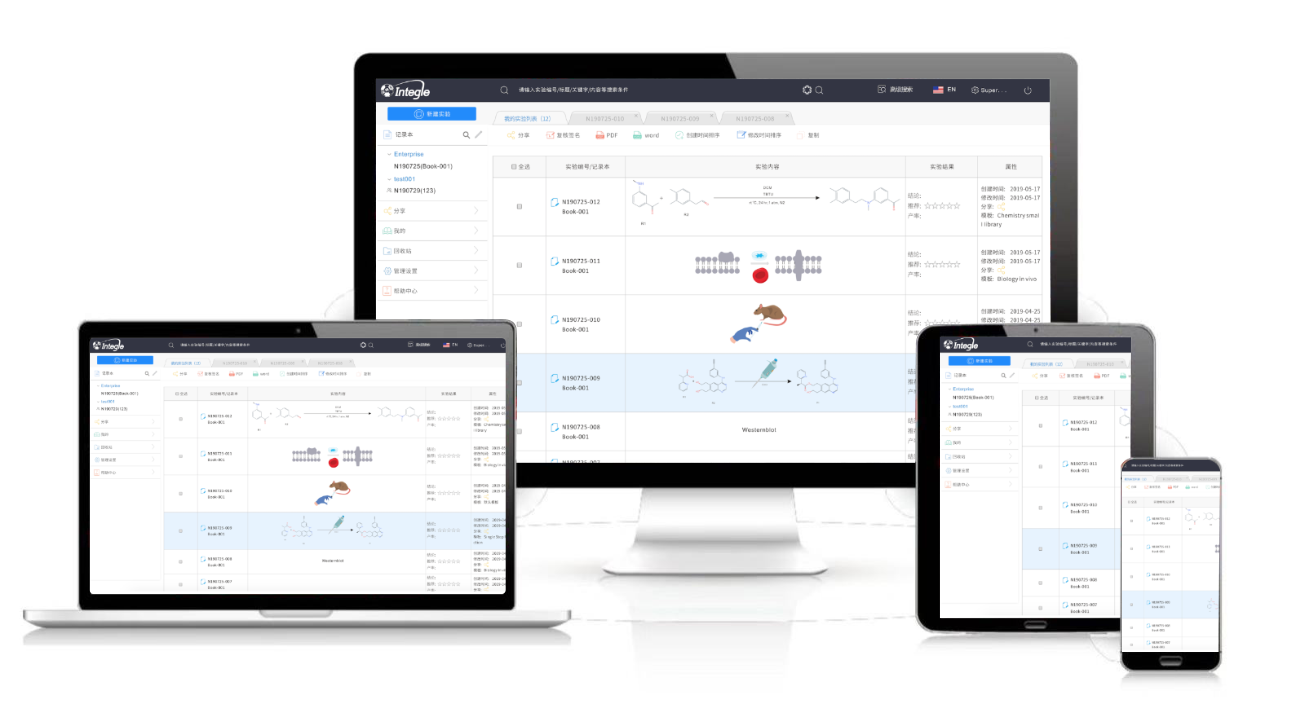
















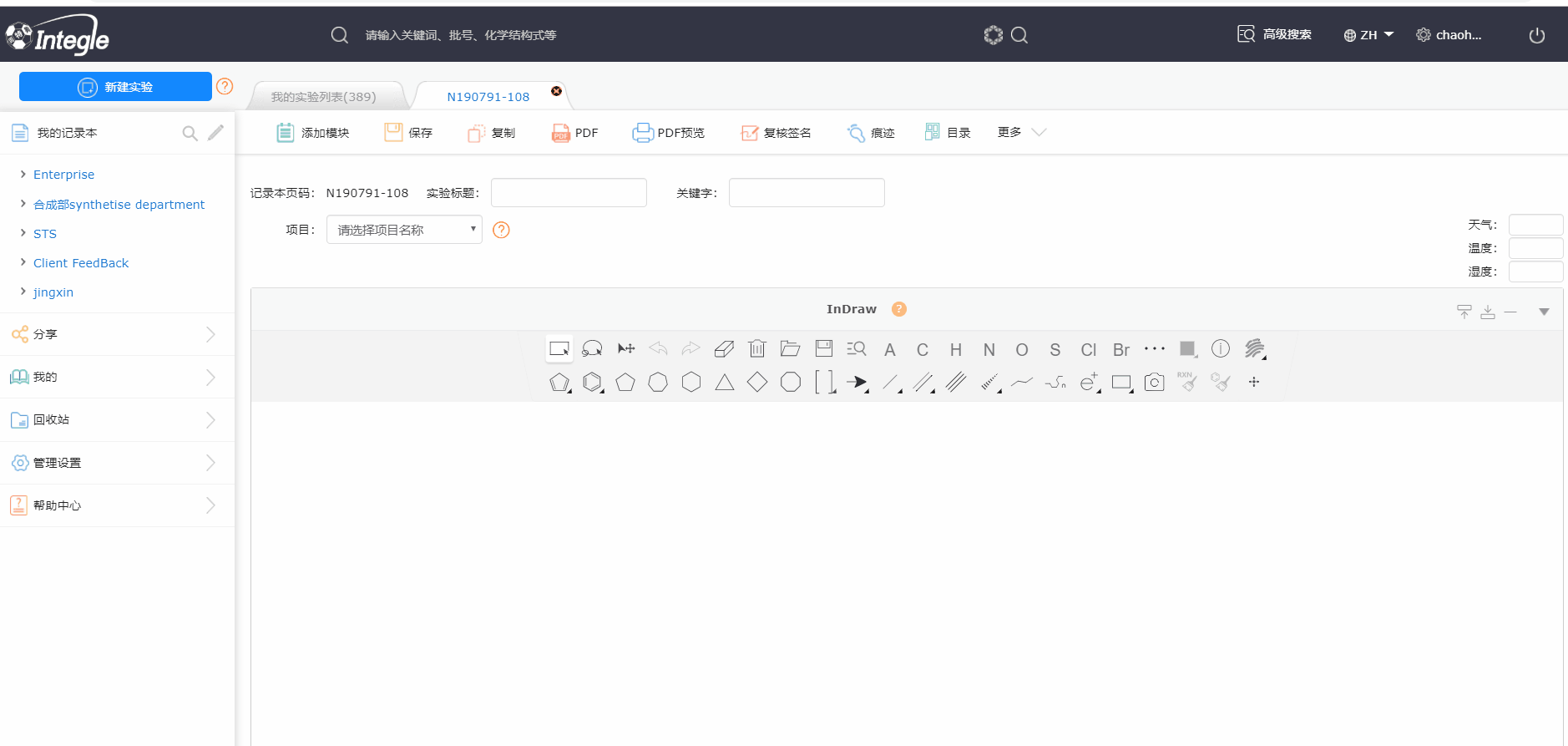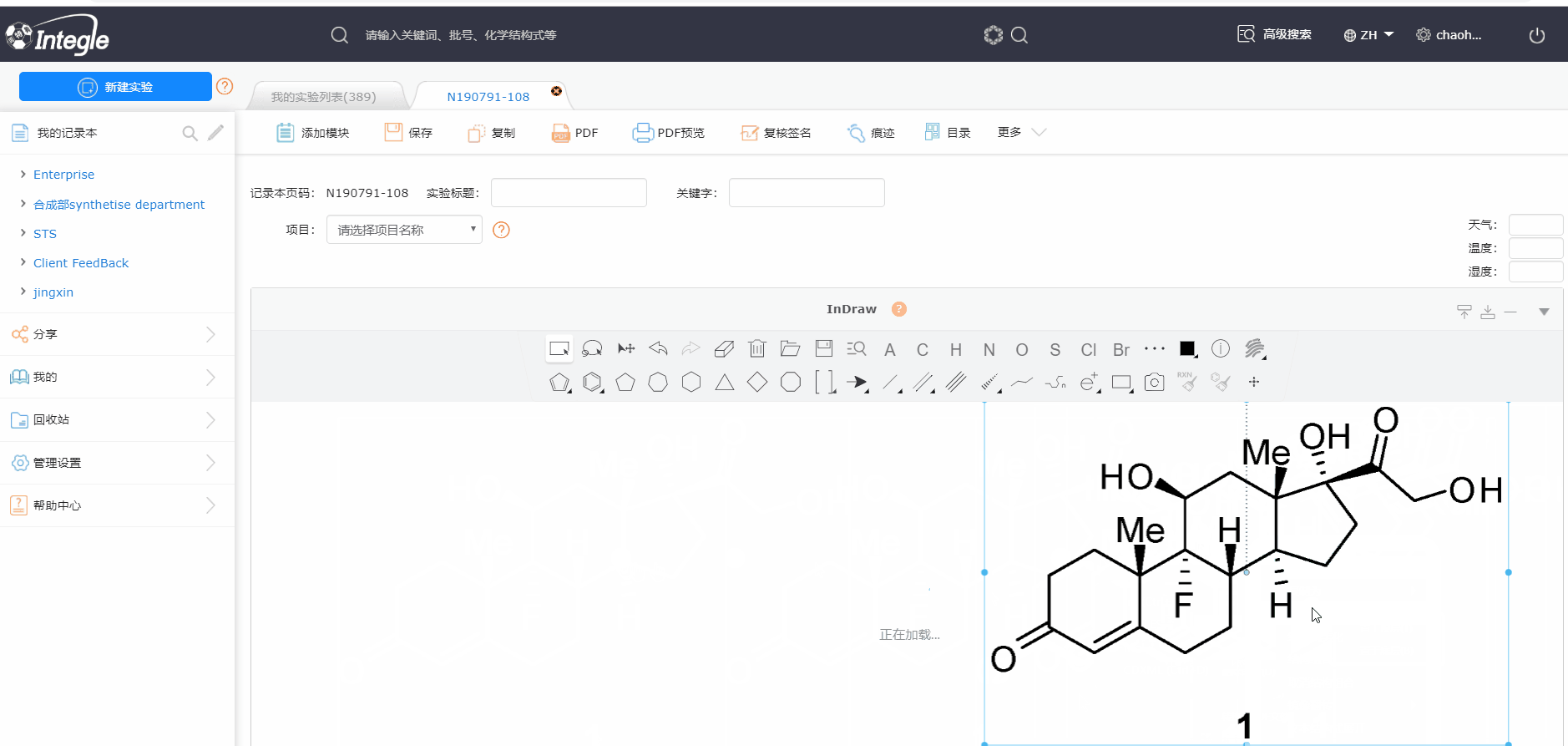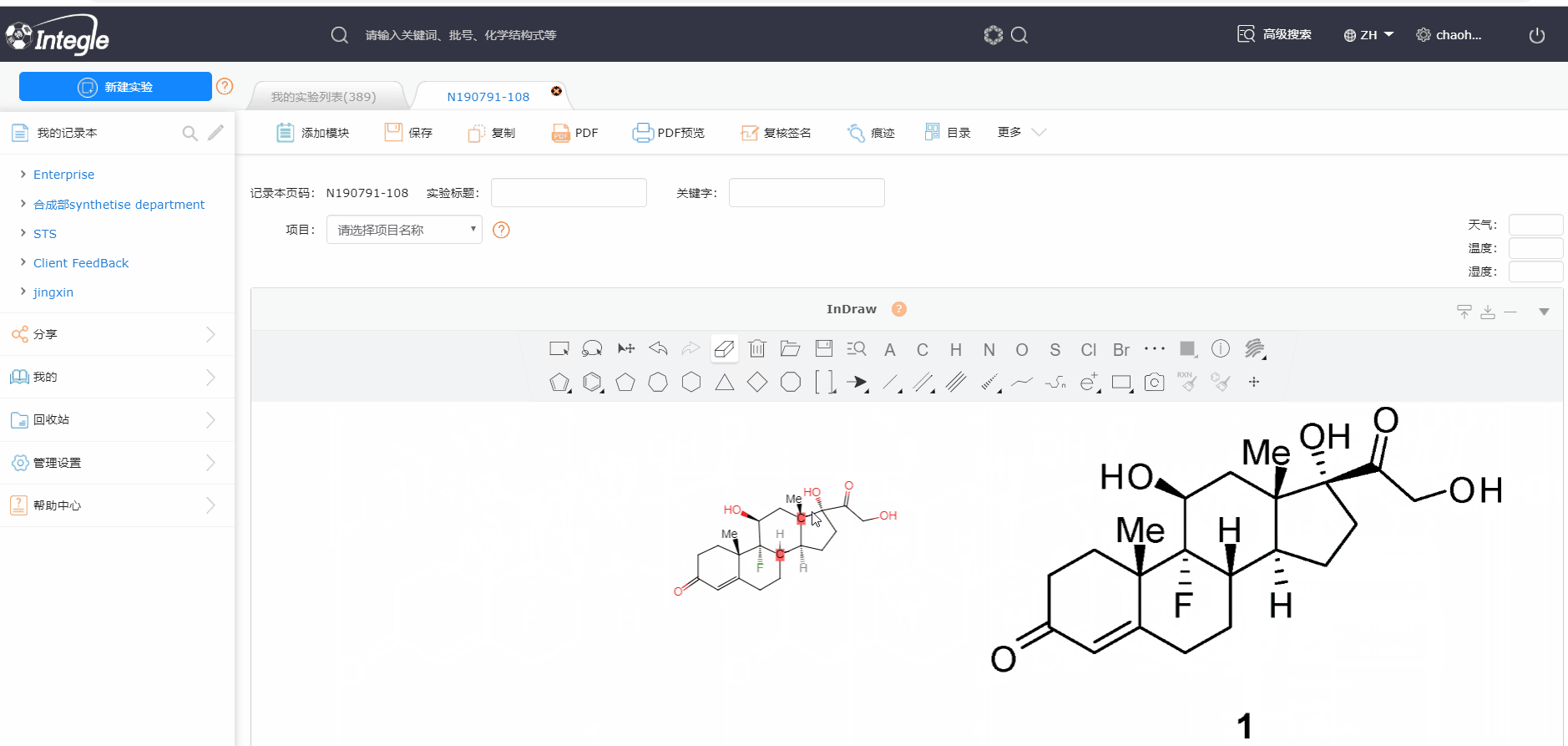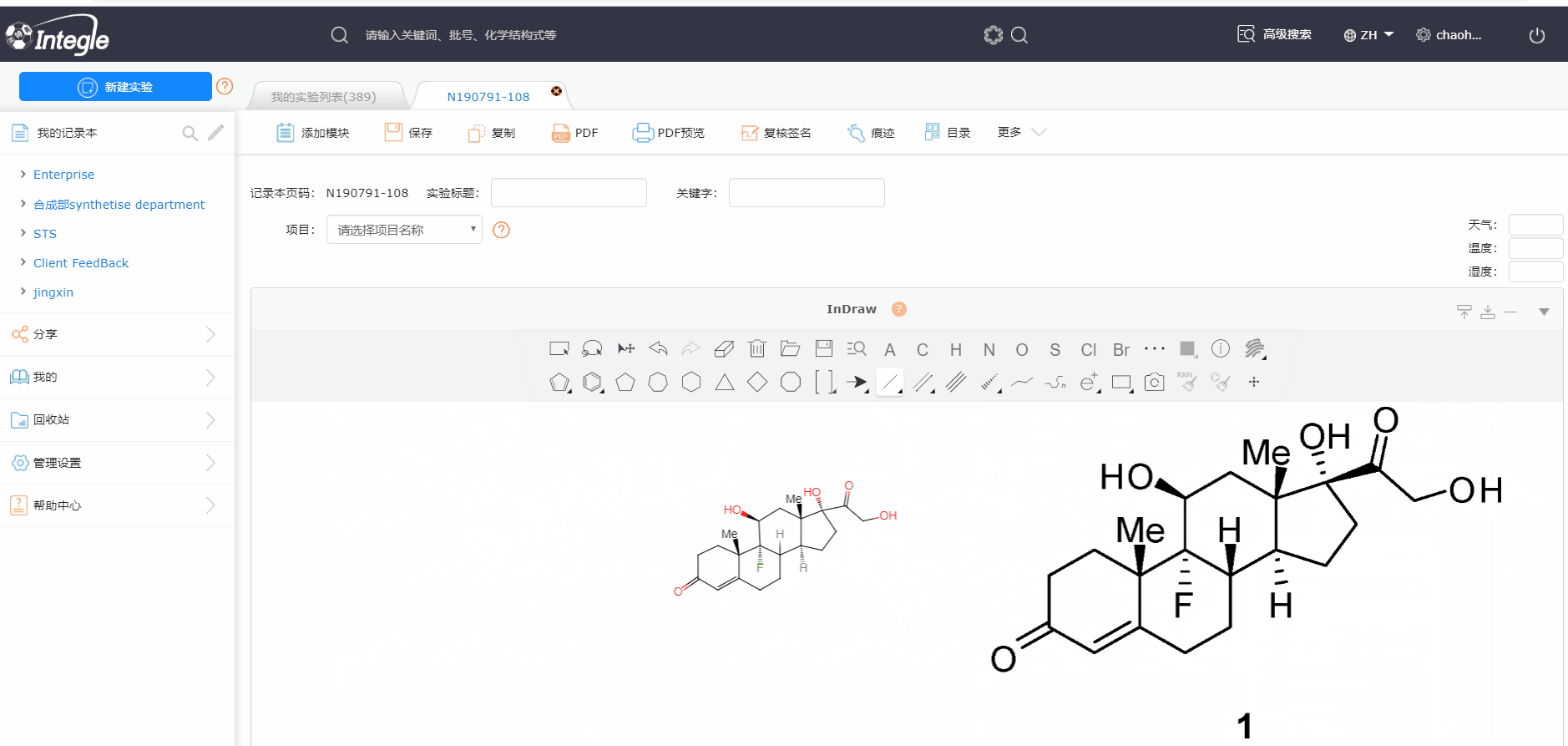
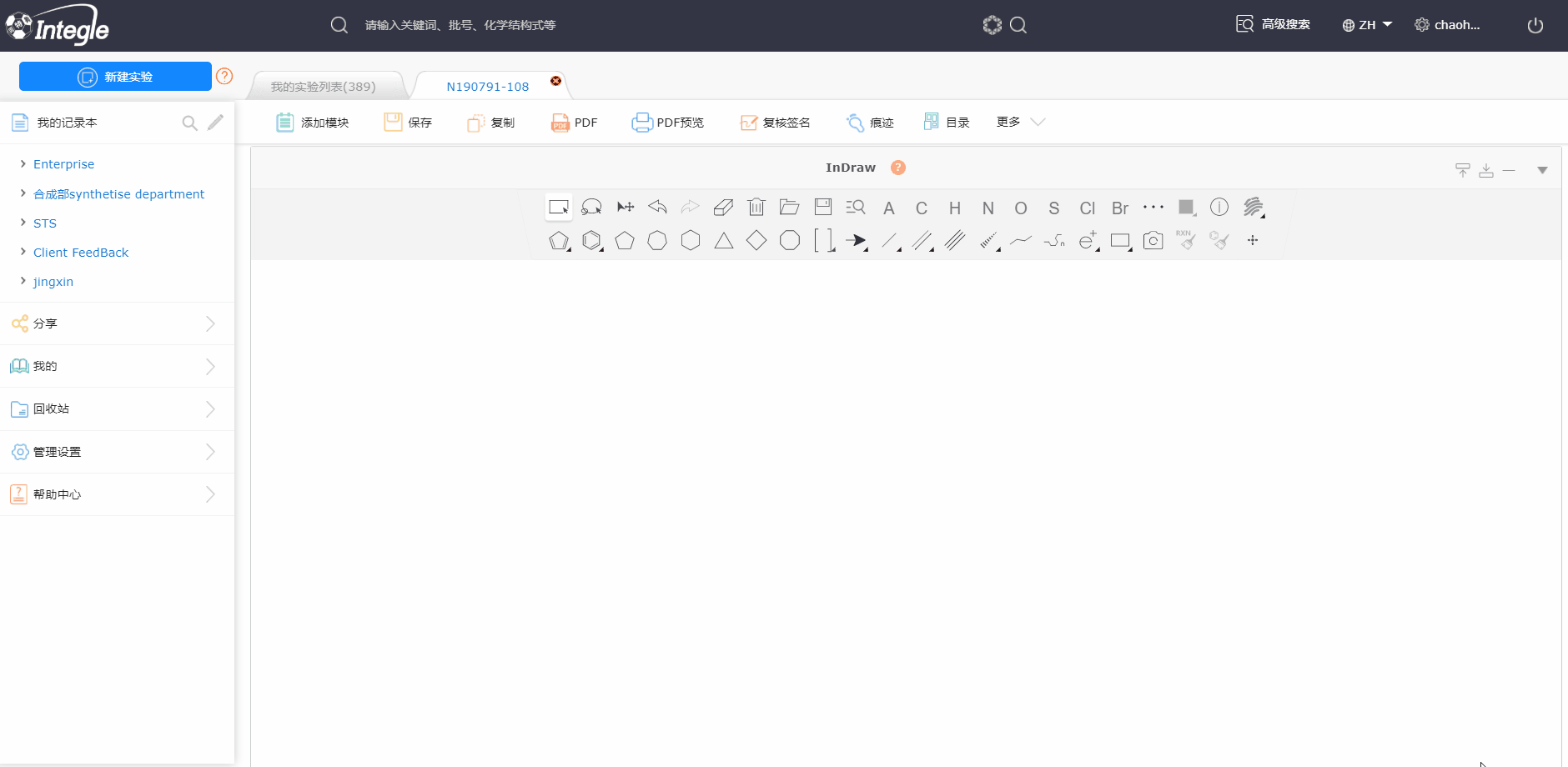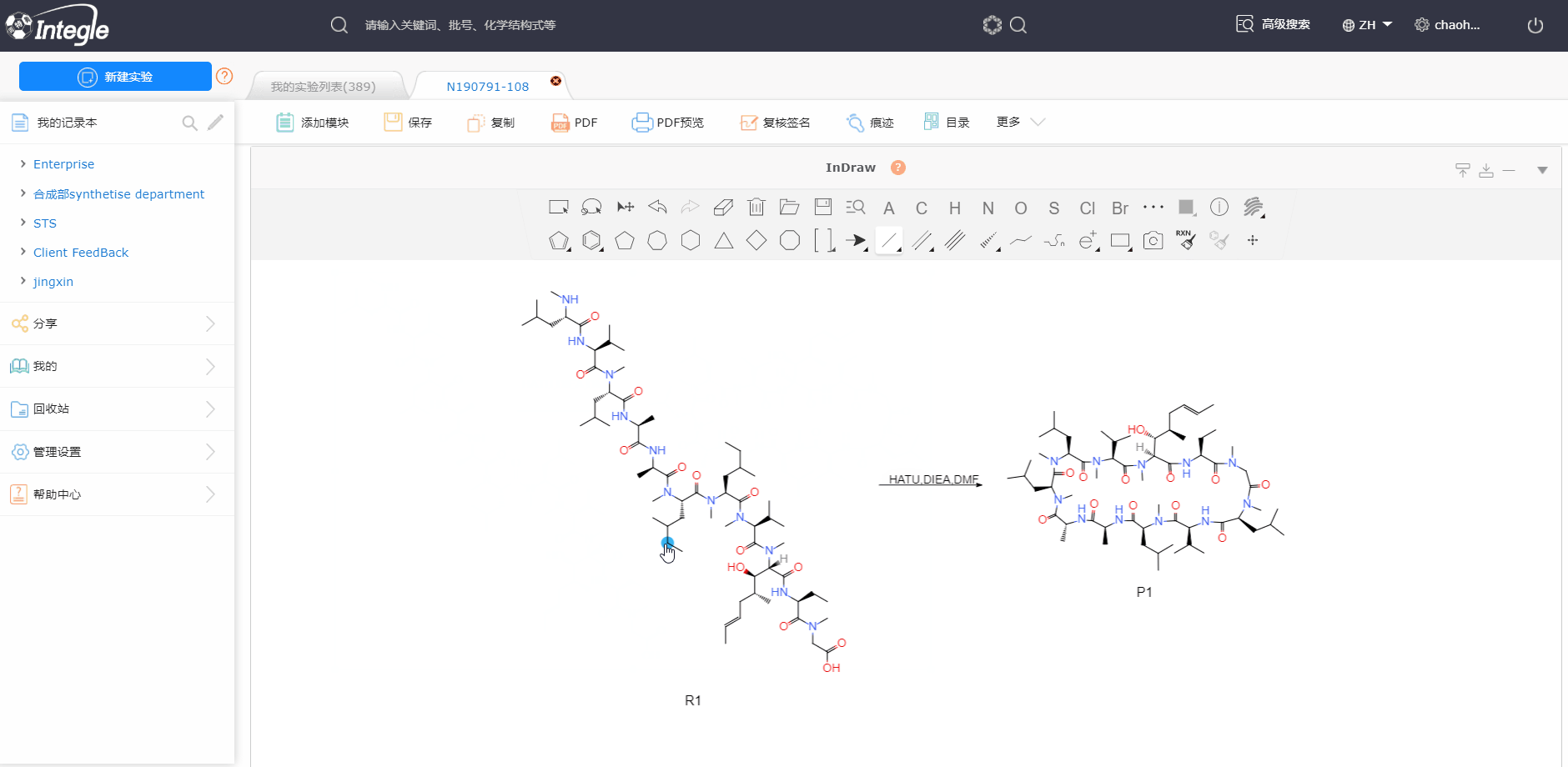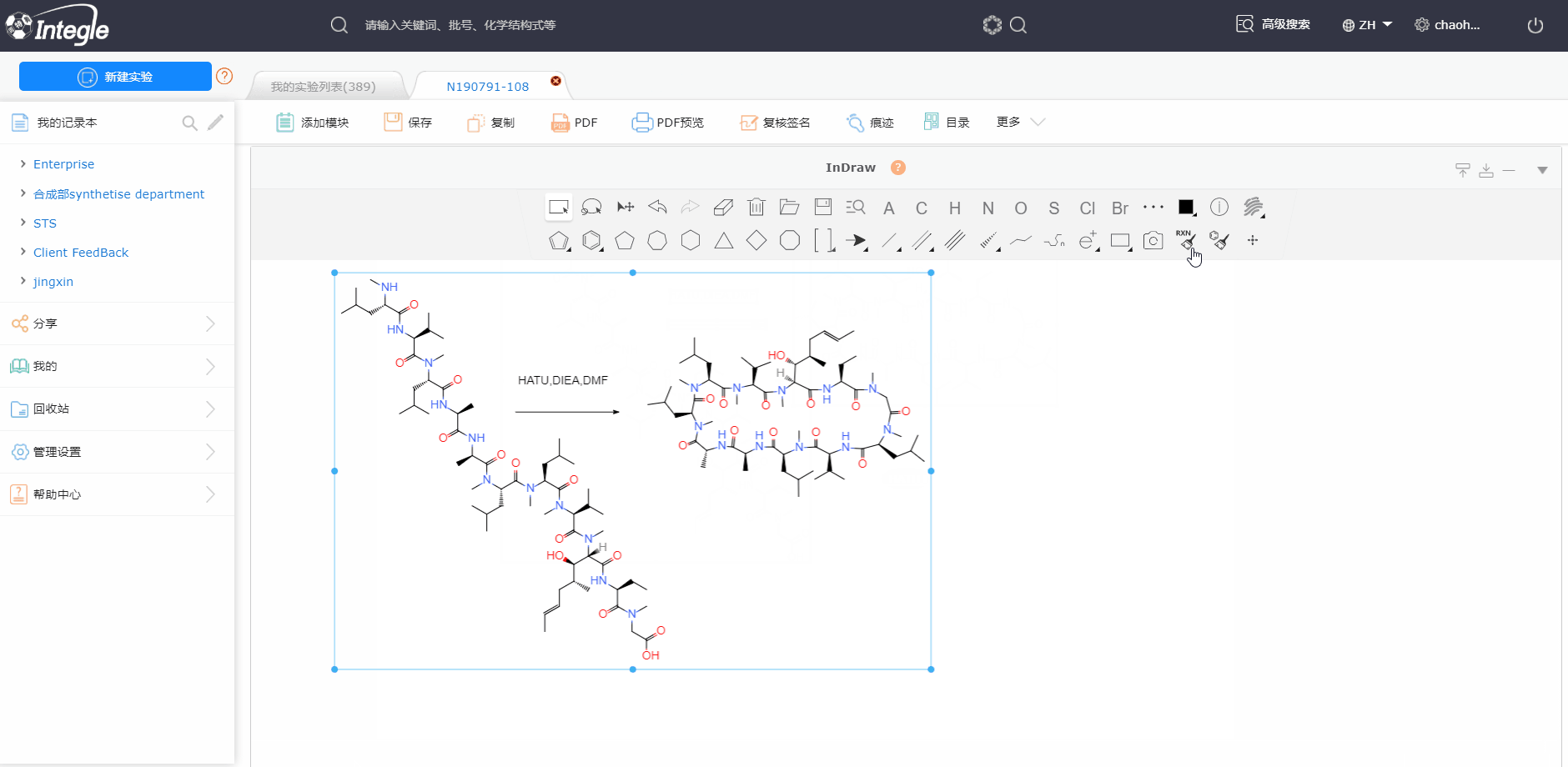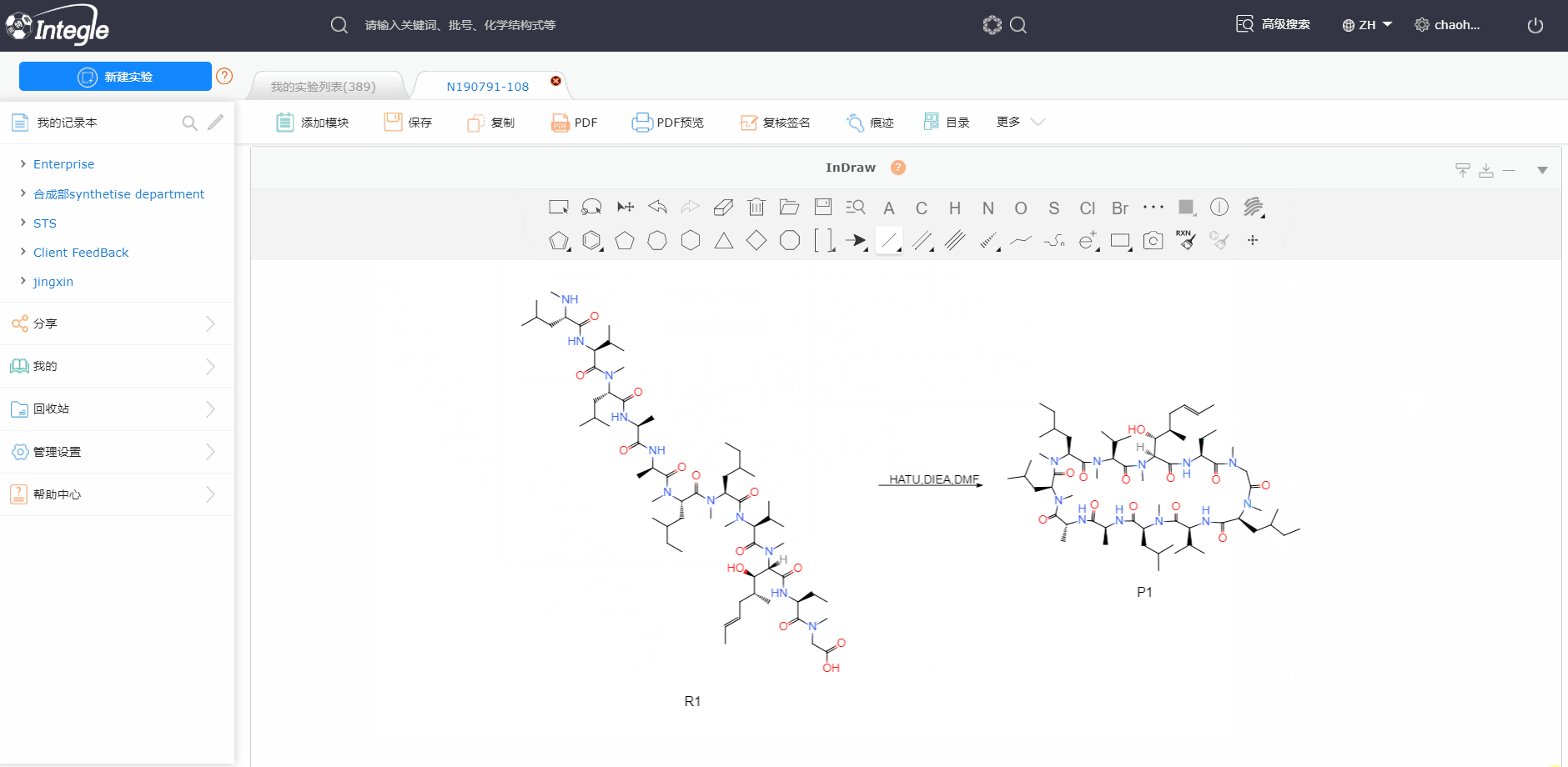


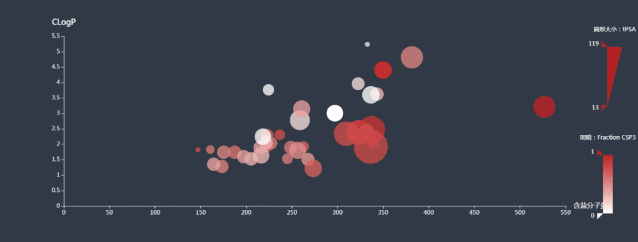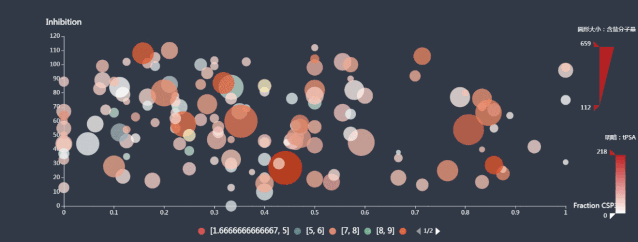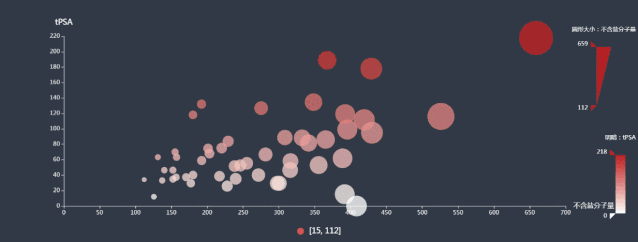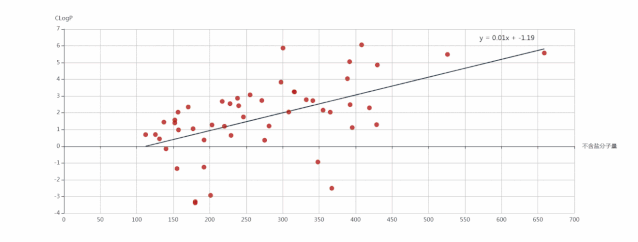
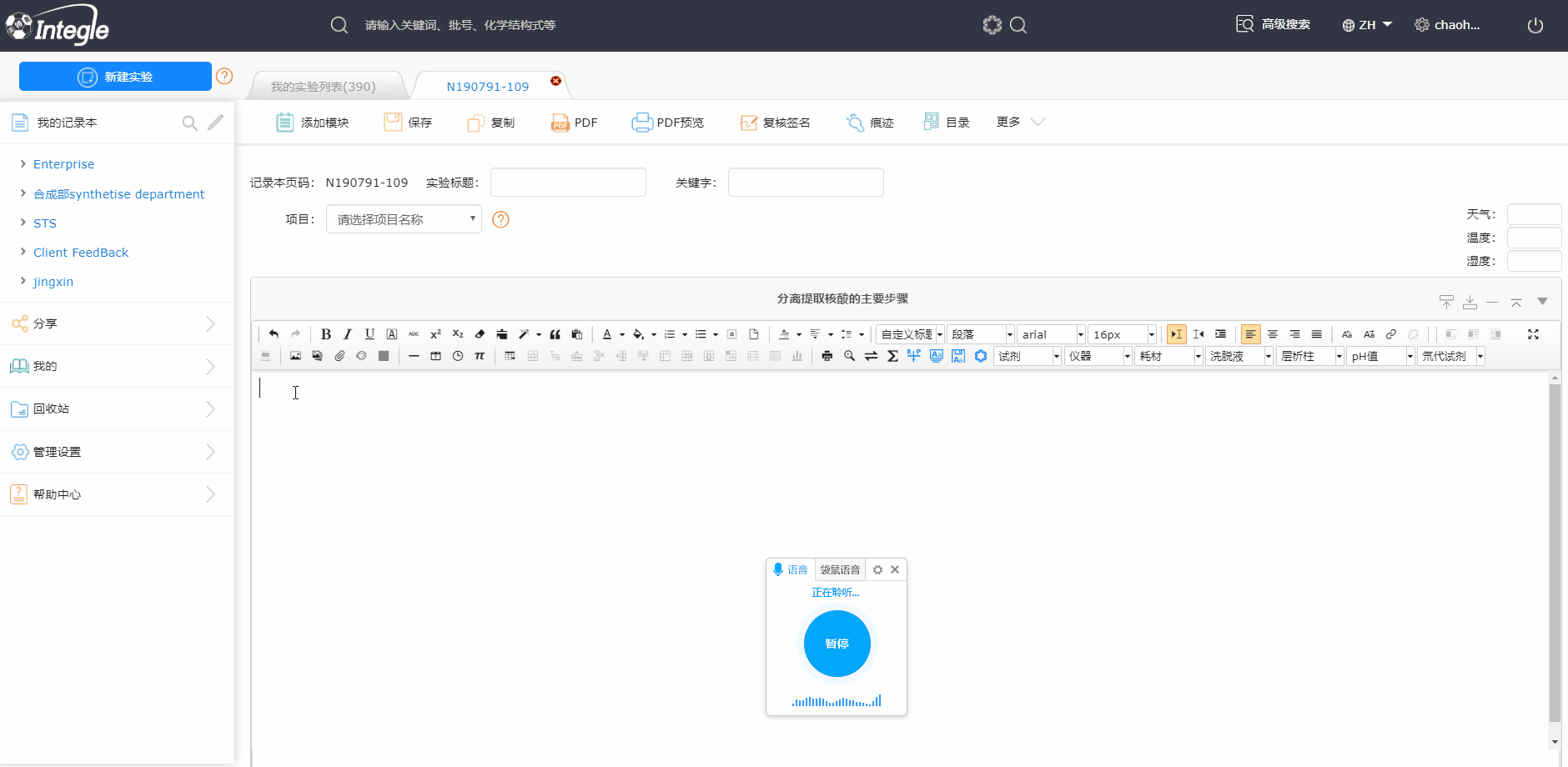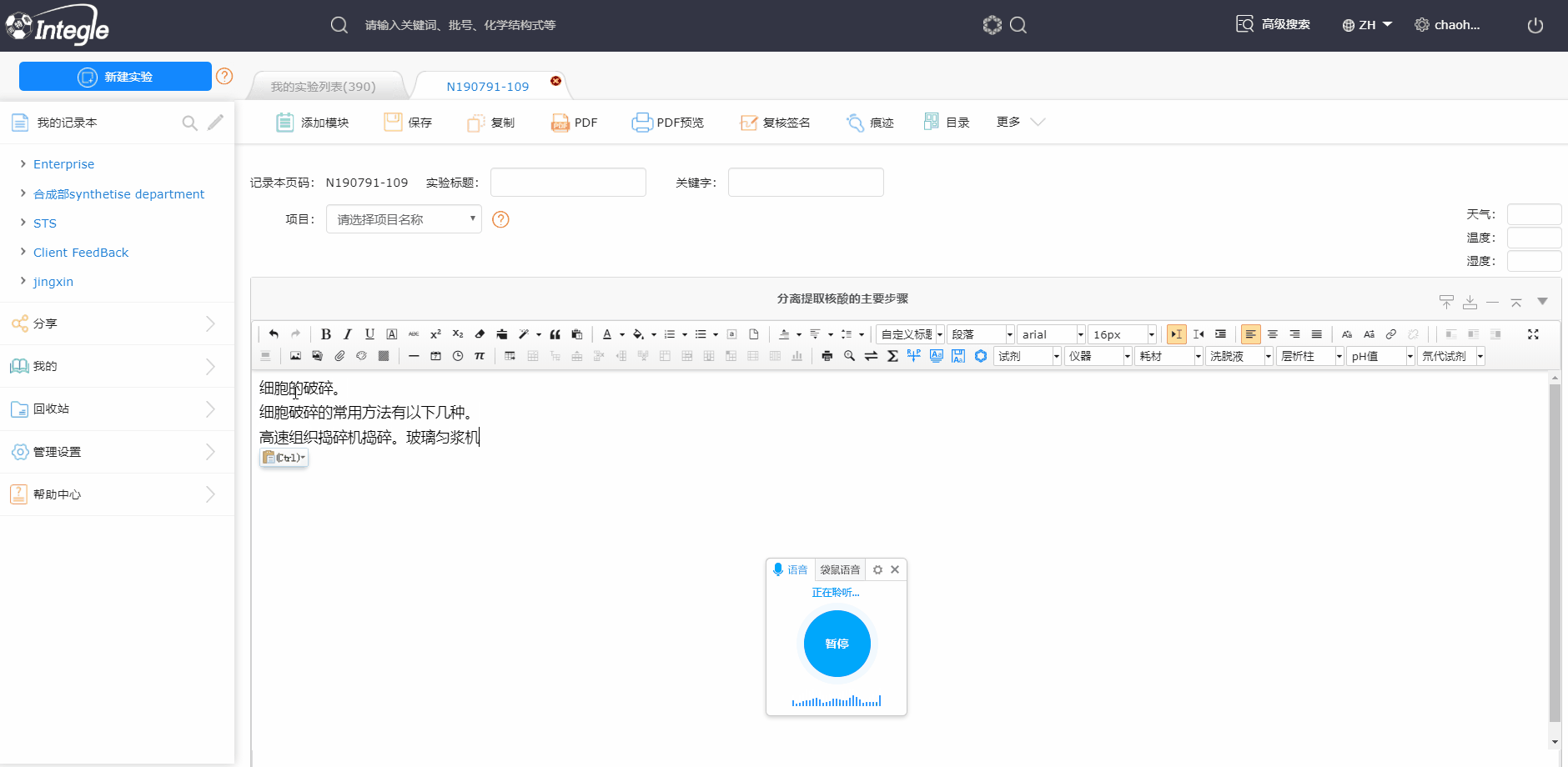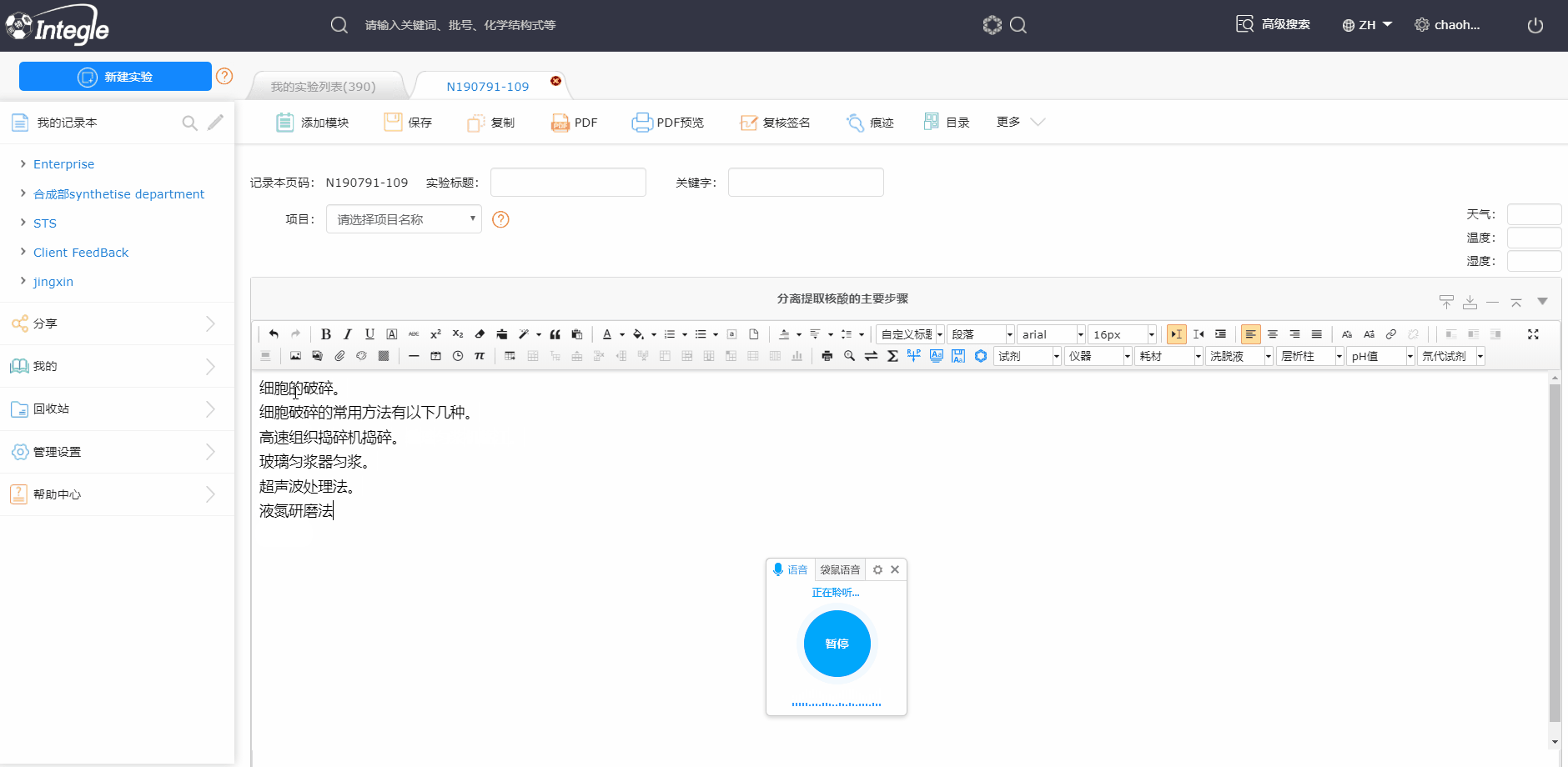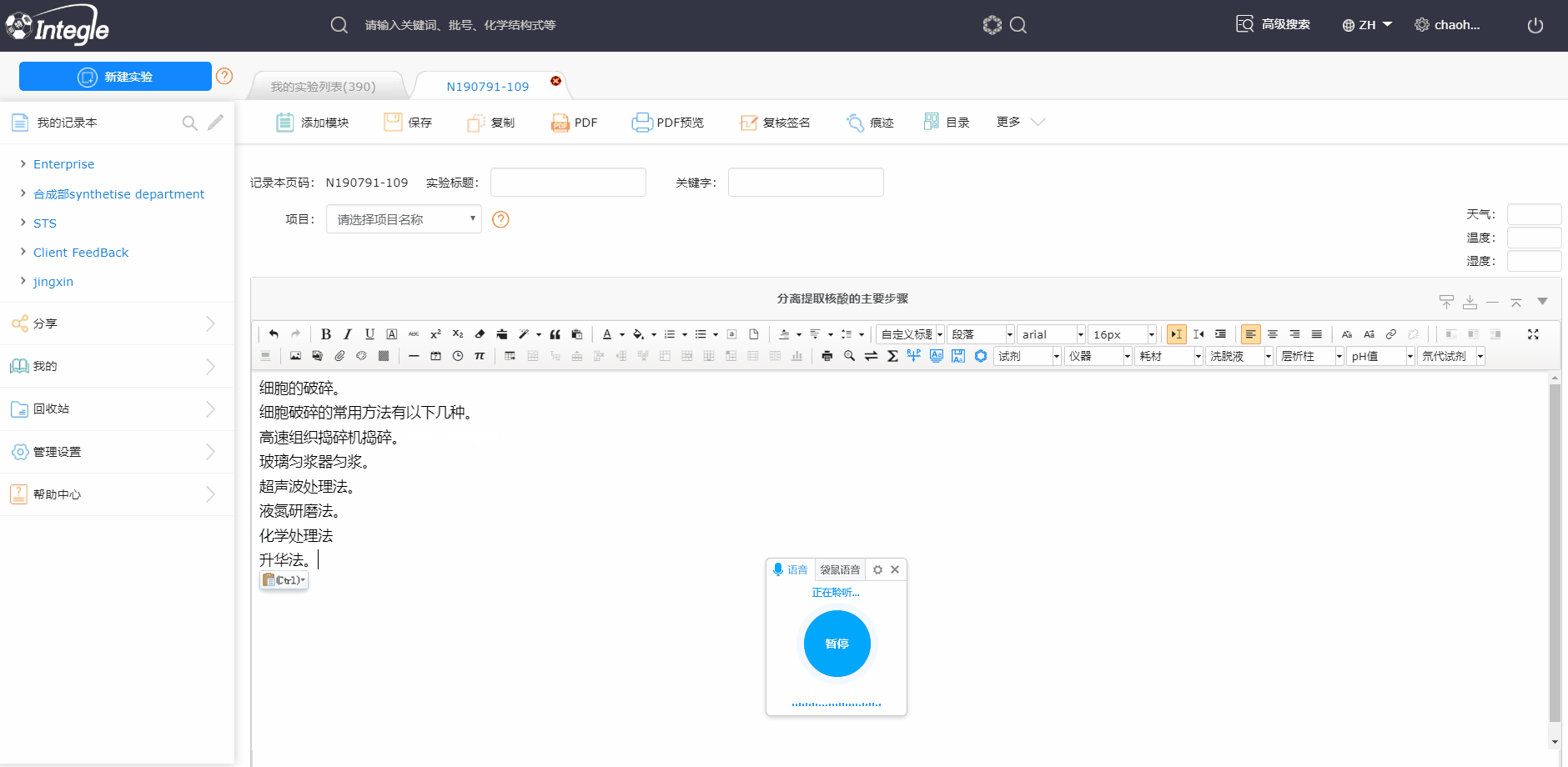


 怎么使用鹰谷电子实验记录本呢?
怎么使用鹰谷电子实验记录本呢? 鹰谷电子实验记录本有哪几种安装部署方式呢?
鹰谷电子实验记录本有哪几种安装部署方式呢? 鹰谷电子实验记录本记录的实验数据可以导出吗?会丢失吗?
鹰谷电子实验记录本记录的实验数据可以导出吗?会丢失吗? 有好几个项目,可以设置管理层能看到所有实验,但是不同项目人员彼此看不到对方的实验吗?
有好几个项目,可以设置管理层能看到所有实验,但是不同项目人员彼此看不到对方的实验吗? 电子实验记录可以代替纸质实验记录吗?合规方面具体满足哪些法规要求呢?
电子实验记录可以代替纸质实验记录吗?合规方面具体满足哪些法规要求呢? ELN和LIMS有什么区别呢?
ELN和LIMS有什么区别呢?
